Como interpretar curvas de TGA e DSC
Clique para receber o guia de interpretação Grátis
1) TERMOGRAVIMETRIA (TGA)
A termogravimetria ou análise termogravimétrica (TGA) é uma técnica da análise térmica na qual a variação da massa da amostra (perda ou ganho) é determinada em função da temperatura e/ou tempo, enquanto a amostra é submetida a uma programação controlada de temperatura.
Esta técnica possibilita conhecer as alterações que o aquecimento pode provocar na massa de substâncias, permitindo estabelecer a faixa de temperatura em que elas adquirem composição química fixa, definida e constante, a temperatura em que começam a decompor, acompanhar o andamento de reações de desidratação (perda de umidade), oxidação, combustão, decomposição, etc (Canevaloro, S. “Técnicas de Caracterização de Polímeros”, Artliber Editora, 2004)).
No método termogravimétrico convencional ou dinâmico, são registradas curvas de massa da amostra (m) em função da temperatura (T) ou do tempo (t), conforme a equação (1):
m = f (T ou t) (1)
Essas curvas são denominadas curvas termogravimétricas ou, simplesmente, curvas de TGA. As curvas de TGA podem e devem ser derivadas (primeira) registrando-se a DTG (termogravimetria derivada) que fornece informações da derivada primeira da variação da massa em relação ao tempo (dm/dt) ou em função da temperatura (dm/dT), conforme equação (2) (Canevaloro, S. “Técnicas de Caracterização de Polímeros”, Artliber Editora, 2004):
dm/dt = f (T ou t) ou dm/dT = f (T ou t) (2)
As Figuras 1 e 2 exemplificam uma curva padrão de TGA e DTG. De acordo com a norma ASTM E 2550-11, a Ti (Temperatura inicial) é a menor temperatura em que pode ser detectado o início da variação de massa para um determinado conjunto de condições experimentais e Tf (Temperatura final) é a menor temperatura indicando que o processo responsável pela variação de massa foi concluído. O início da inflexão da curva da DTG (início do pico de DTG) pode ser usado para ajudar a identificar a Ti e a Tf (final do pico de DTG). A Tonset é identificada pelo cruzamento entre as linhas a e b, e é denominada de início extrapolado ou início matemático.
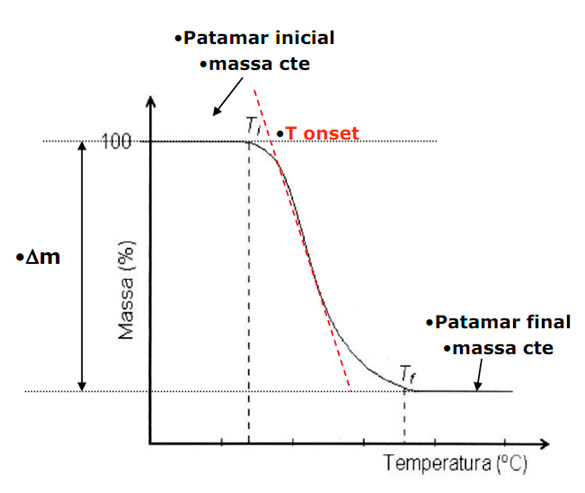
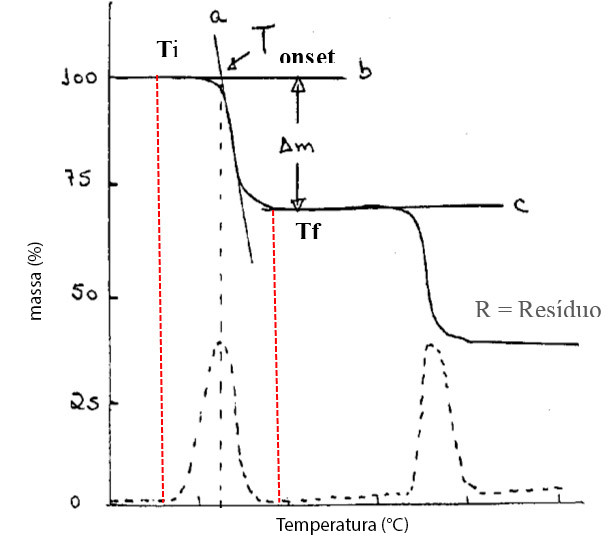
Figura 1: Curva de decomposição térmica de um material.
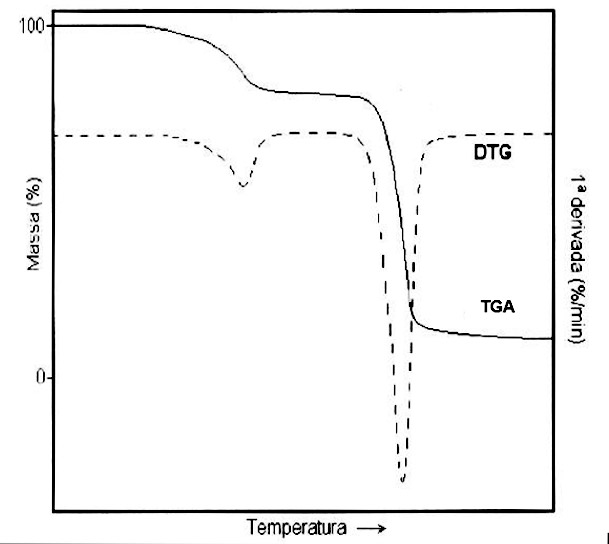
Figura 2: Curva teórica da decomposição térmica de um material: TGA – curva termogravimétrica e DTG – derivada da curva TGA.
Toda curva de TGA deve ser analisada com auxílio da curva de DTG. Com a curva de DTG é possível identificar em quantas etapas ocorre uma decomposição térmica ou uma degradação termo-oxidativa.
Por exemplo, na Figura 3, a curva (a) é correspondente à de uma reação que ocorre numa única etapa e numa estreita faixa de temperatura; a curva (b) consiste de duas reações que são parcialmente sobrepostas; a curva (c) representa duas reações, a primeira ocorrendo lentamente (I) e que é seguida por outra (II), que ocorre rapidamente; e a curva (d) corresponde a uma série de reações secundárias ou menores que ocorrem simultaneamente ou próximas à reação principal.
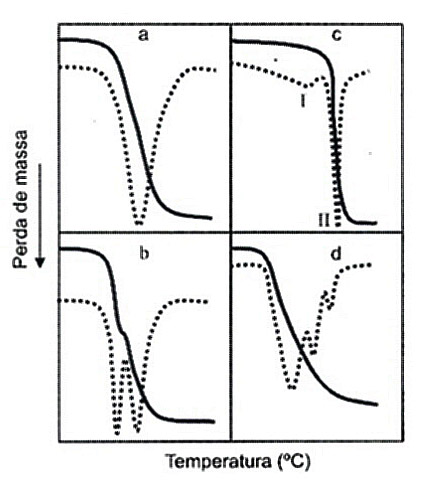
Figura 3: Curvas teóricas da decomposição térmica de um material: linha cheia- TGA e linha pontilhada – DTG.
2) DSC
A calorimetria exploratória diferencial (DSC) é utilizada para medir a diferença de energia entre uma amostra e um material de referência em função de um programa de aquecimento ou resfriamento sob atmosfera controlada. Geralmente é utilizada para determinar a temperatura de fusão e cristalização; entalpias de fusão e de cristalização, bem como na determinação da temperatura de transição vítrea.
Assim, o equipamento de DSC mede a variação de energia entre a amostra e uma determinada referência em função da temperatura e/ou tempo, enquanto a amostra é submetida a uma programação controlada de temperatura. Os eventos térmicos que geram modificações em curvas de DSC podem ser basicamente transições de primeira e de segunda ordem. As transições de primeira ordem apresentam variações de entalpia – endotérmica ou exotérmica – e dão origem à formação de picos. Como exemplos de eventos endotérmicos que podem ocorrer em amostras de materiais, pode-se citar: fusão, perda de massa da amostra (vaporização de água, aditivos ou produtos voláteis de reação ou de decomposição), dessorção e reações de redução. Eventos exotérmicos podem ser: cristalização, reações de polimerização, cura, oxidação, degradação oxidativa, adsorção, entre outros. As transições de segunda ordem caracterizam-se pela variação de capacidade calorífica, porém sem variações de entalpia. Assim, estas transições não geram picos nas curvas de DSC, apresentando-se como um deslocamento da linha base em forma de S. Exemplos característicos são a transição vítrea e relaxações de tensões térmicas da cadeia polimérica.
Existem, basicamente, dois tipos de equipamentos de calorimetria exploratória diferencial: o DSC que trabalha com o princípio de operação de compensação de potência e o DSC que possui a operação baseada no princípio de fluxo de calor. Incondicionalmente, as grandezas físicas obtidas dos testes realizados em quaisquer dos tipos de instrumentos são as mesmas, como mostra a Figura 4.
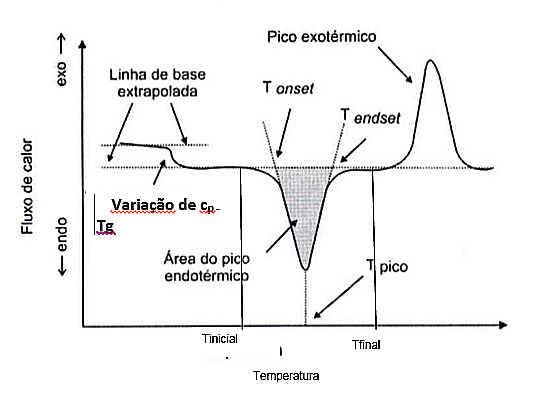
Figura 4: Tipos de eventos térmicos registrados pelo DSC (adaptado Canevaloro, S. “Técnicas de Caracterização de Polímeros”, Artliber Editora, 2004)
A fusão é uma transição de primeira ordem, característica de metais, materiais cristalinos e polímeros semicristalinos. Essa transição pode ocorrer em uma temperatura determinada quando o material for altamente cristalino (pico estreito e de grande amplitude) ou ocorrer em uma faixa de temperatura, devido à distribuição de tamanho das regiões cristalinas presentes nas macromoléculas. A temperatura na qual desaparece totalmente a cristalinidade é referida como ponto de fusão do material e corresponde, aproximadamente, ao máximo do pico de fusão na curva de DSC. O calor de fusão ou entalpia de formação pode ser determinado pela área contida sob o pico endotérmico, relacionando-a com a massa de amostra utilizada. As normas ASTM para determinar a temperatura e a entalpia de fusão são as ASTM E 794-06 e E793-06.
O processo de cristalização é contrário ao de fusão, ou seja, é acompanhado de liberação de calor latente, que gera um pico exotérmico bem definido na curva de DSC. A taxa de resfriamento utilizada na cristalização do material afeta diretamente a forma, a altura e a energia do pico exotérmico no DSC. As normas ASTM para determinar a temperatura e a entalpia de cristalização são as ASTM E 794-06 e E793-06.




